Теплоёмкость и количество теплоты
1. Теплообмен и теплопередача
Изменить внутреннюю энергию газа в цилиндре можно, не только совершая работу, но и нагревая газ.
Если закрепить поршень, то объем газа при нагревании не меняется и работа не совершается.
Но температура газа, а следовательно, и его внутренняя энергия возрастают.
Процесс передачи энергии от одного тела к другому без совершения работы называют теплообменом или теплопередачей.
Виды теплопередачи:
1) излучение
2) конвенция
3) теплопроводность
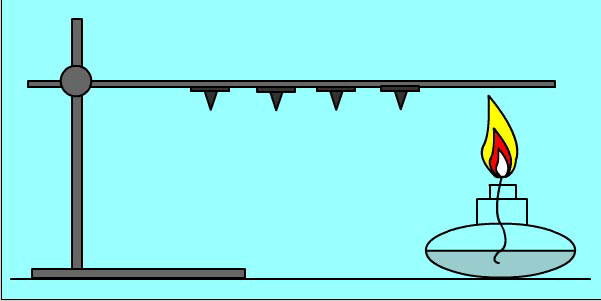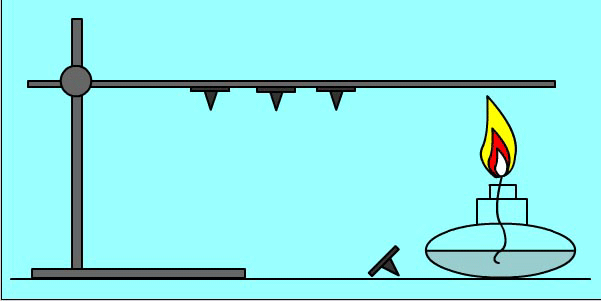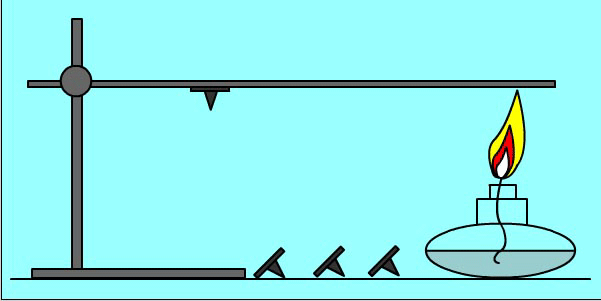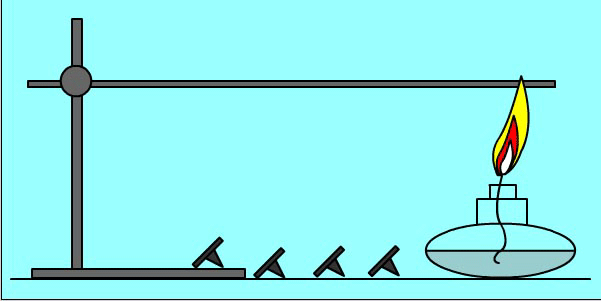
Теплопередача - самопроизвольный процесс. Опыт: кнопки прикреплены к металлическому пруту парафином. При нагревании парафин плавится и кнопки отваливаются.
2. Понятие количество теплоты
Количественную меру изменения внутренней энергии при теплообмене называют количеством теплоты. Количеством теплоты называют также энергию, которую тело отдает в процессе теплообмена.
Количеством теплоты обозначается буквой - Q.
Количество теплоты – это физическая величина, показывающая, какая энергия передана телу в результате теплообмена.
В международной системе единицей количества теплоты, также как работы и энергии, является джоуль: [Q] = [A] = [E] = 1 Дж.
На практике еще иногда применяется внесистемная единица количества теплоты – калория. 1 кал. = 4,2 Дж.
Молекулярная картина теплообмена.
При теплообмене на границе между телами происходит взаимодействие медленно движущихся молекул холодного тела с быстро движущимися молекулами горячего тела. В результате кинетические энергии молекул выравниваются и скорости молекул холодного тела увеличиваются, а горячего — уменьшаются.
При теплообмене не происходит превращения энергии из одной формы в другую, часть внутренней энергии горячего тела передается холодному телу.
Количество теплоты при теплообмене
Количество теплоты, передаваемое от одного тела к другому, может идти на нагревание тела, плавление, парообразование, либо выделяться при противоположных процессах – остывании тела, кристаллизации, конденсации. Теплота выделяется при сгорании топлива.
Между массой вещества и количеством теплоты, необходимым для его нагревания, существует прямая пропорциональная зависимость.
Количество теплоты, необходимое для нагревания тела или выделяющееся при его охлаждении, прямо пропорционально массе тела и изменению его температуры.
Q = cmΔT
Количество теплоты, необходимое для превращения жидкости в пар или выделяющееся при его конденсации, прямо пропорционально массе жидкости.
Q = rm
Количество теплоты, необходимое для плавления тела или выделяющееся при его кристаллизации, прямо пропорционально массе этого тела.
Q = λm.
Количество теплоты, выделяющееся при сгорании топлива, прямо пропорционально его массе.
Q = qm
3. Теплоемкость
Теплоемкость термодинамической системы называют количество теплоты, которое нужно сообщить т.д.с, чтобы изменить ее температуру на 10С.
Для газов удобно пользоваться молярной теплоемкостью.
Молярной теплоемкостью системы называют количество теплоты, которое нужно сообщить одному молю идеального газа, чтобы изменить ее температуру на 10С.
[Cμ] = Дж/(моль×К).
Формулы связи:
Во всех формулах, позволяющих рассчитывать количество теплоты для различных тепловых процессов, стоят коэффициенты пропорциональности, называемые удельными величинами, то есть приходящимися на единицу других величин. Удельные величины являются характеристиками веществ, а не тел.
Удельная теплоемкость вещества показывает, чему равно количество теплоты, необходимое для нагревания или выделяющееся при охлаждении 1 кг вещества на 1 К.
Удельные теплоты парообразования, плавления, сгорания показывают, какое количество теплоты требуется для парообразования, плавления или выделяется при конденсации, кристаллизации, сгорании 1 кг вещества.
Чтобы получить единицы удельных величин, их надо выразить из соответствующих формул и в полученные выражения подставить единицы теплоты – 1 Дж, массы – 1 кг, а для удельной теплоемкости – и 1 К.
Получаем единицы: удельной теплоемкости – 1 Дж/кг·К, остальных удельных теплот: 1 Дж/кг.
Формулы связи: Сμ= μ·с С= m·с
Если одинаковым по массе телам из разных веществ передать одно и тоже количество теплоты, то они нагреются до разной температуры. Вещество с меньшей теплоемкостью нагреется сильнее, а вещество с большей - слабее.
Теплоемкость при постоянном давлении и объеме
Теплоемкость различается в зависимости от того, при каких условиях происходит нагревание тела — при постоянном объеме или при постоянном давлении.
Если нагревание тела происходит при постоянном объеме, т.
е. ΔV = 0, то работа равна нулю. В этом случае передаваемое телу тепло
идет только на изменение его внутренней энергии, ΔQ = ΔU,
и в этом случае молярная теплоемкость равна изменению внутренней энергии при
изменении температуры на 1 К, т. е.
.
Поскольку для газа
Эта формула определяет теплоемкость 1 моля идеального газа, называемую молярной.
Удельная теплоемкость при постоянном давлении равна
Теплоемкость при постоянном давлении
При нагревании газа при постоянном давлении его объем меняется, сообщенное телу тепло идет не только на увеличение его внутренней энергии, но и на совершение работы, т.е. ΔQ = ΔU + PΔ V.
Молярная теплоемкость при постоянном давлении
Для идеального газа PV = RT и поэтому PΔV = RΔT.
Учитывая это, найдем
Молярная теплоемкость при постоянном давлении
Удельная теплоемкость при постоянном давлении равна
.
Формула Майера.
Для любого идеального газа справедливо соотношение Майера:
Cpμ – CVμ = R,
где R — универсальная газовая постоянная,
Cpμ — молярная теплоемкость при постоянном давлении,
CVμ — молярная теплоемкость при постоянном объёме
Отношение
представляет
собой величину, характерную для каждого газа и определяемую числом степеней
свободы молекул газа.
Примеры решения задач:
Задача 1. Вычислить удельные теплоемкости cV и cp газов: 1) гелия; 2) водорода; 3) углекислого газа.
Задача 2:. Разность удельных теплоемкостей cp-cV некоторого двухатомного газа равна 260 Дж/(кг*К). Найти молярную массу M газа и его удельные теплоемкости cV и cp.
Задача 3. В камеру сгорания закачана смесь из двух молей водорода и одного моля кислорода при давлении р = 1МПа и температуре t = 20ºC. Определить массовые доли содержания компонентов смеси, молярную массу смеси, газовую постоянную, теплоемкость смеси.
Дано:
ν1 = 2моль
ν2 = 1моль
1. по таблице Менделеева находим:
По таблице Менделеева находим молярную массу вещества
μ1 = 2,0159·10-3 кг/моль - водород
μ2 = 31,9968·10-3 кг/моль - кислород
2. Вычислите газовые постоянные газов, используя значения универсальной газовой постоянной R=8,31 Дж/моль·К
cpсм= g1· cp1+ g2· cp2 = 2,4·103
Теплоемкость при постоянном объеме:
сv1 = cp1 – R1 = 10,28·103
сv2 = cp2 – R2 = 0,641·103
сvсм = cpсм – Rсм = 1,7·103
Задача 4. Определить количество теплоты, поглощаемой водородом массой m=0,2 кг при нагревании его от температуры t1=0 °С до температуры t2= 100 °С при постоянном давлении. Найти также изменение внутренней энергии газа.
Задачи для самостоятельного решения
1. Смешали 30л воды при 250С и 15л воды при 700С. Определите температуру смеси.
2. В калориметр с теплоемкостью 63 Дж/К было налито 250 г масла при 12 °С. После опускания в масло медного тела массой 500 г при 100 °С установилась общая температура 32°С. Какова удельная теплоемкость масла по данным опыта?
3. Для приготовления ванны вместимостью 200 л смешали холодную воду при 10 °С с горячей при 60 0С. Какие объемы той и другой воды надо взять, чтобы температура установилась 40 °С?
Домашнее задание:
Контрольные вопросы:
1. Что называют количеством теплоты?
2. От чего зависит удельная теплоемкость вещества?
3. Что называют удельной теплотой парообразования?
4. Что называют удельной теплотой плавления?
5. В каких случаях количество теплоты положительная величина, а в каких случаях отрицательная?
Задача:
В сосуд, содержащий 1,5 кг воды при 15 °С, впускают 200 г водяного пара при 100°С. Какая общая температура установится после конденсации пара?