1. Предмет термодинамики и его связь с другими отраслями знаний.
Дисциплина «Термодинамика, теплопередача и гидравлика»
Наука теплотехника включает:

Что изучает теплотехника?
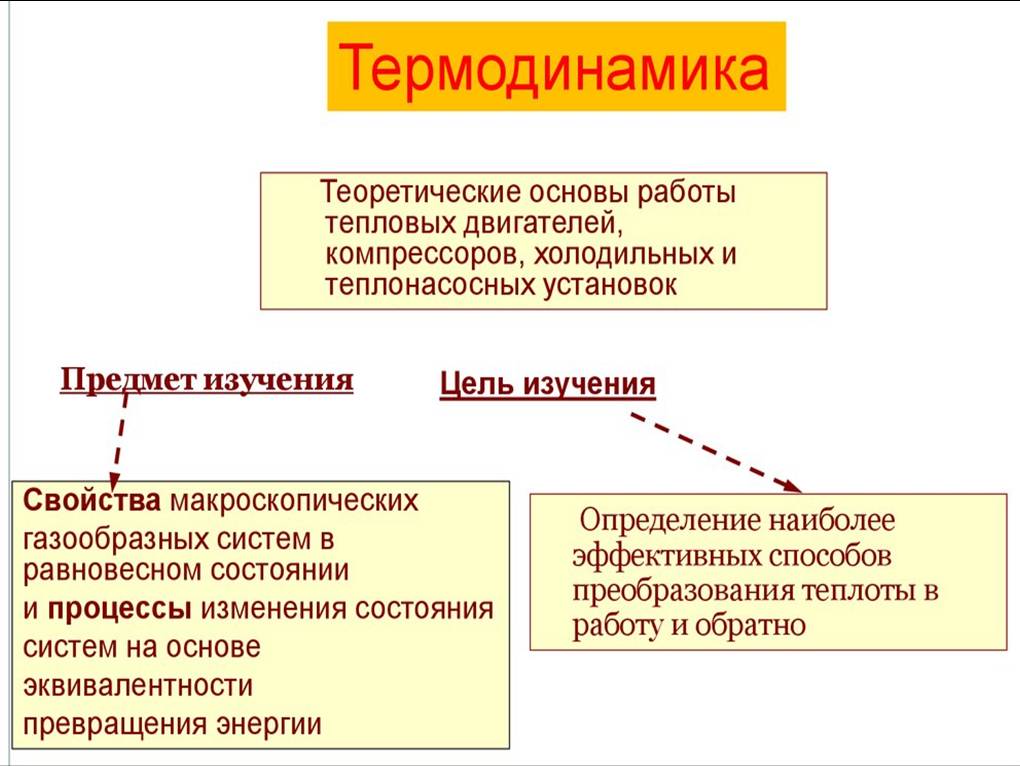
Термодинамика – это раздел, изучающий взаимные превращения теплоты и работы в равновесных системах и при переходе к равновесию. В термодинамике не обязательно знать механизм происходящих процессов, и скорость с которой они протекают, здесь важны лишь начальные и конечные состояния изучаемой системы, а не путь перехода системы из одного состояния в другое.
Термодинамические расчеты являются альтернативой дорогостоящему эксперименту, они позволяют сократить материальные и временные затраты при разработке новых материалов и технологических схем. С их помощью можно предсказать результат поведения веществ при очень высоких или низких температурах и давлениях.
Основным преимуществом термодинамики при решении прикладных задач является ее универсальность - объекты могут быть самыми разными, при этом способы прогнозирования их поведения оказываются одними и теми же.
1. Термодинимика – как наука
Термодина́мика (греч. θέρμη — «тепло», δύναμις — «сила») — раздел физики, изучающий соотношения и превращения теплоты и других форм энергии. Термодинамика — это феноменологическая наука, опирающаяся на обобщения опытных фактов. Она изучает макроскопические системы, состоящие из огромного числа частиц —термодинамические системы.
Процессы, происходящие в таких системах, описываются макроскопическими величинами, такими как давление или температура, которые не применимы к отдельным молекулам и атомам.
Современная феноменологическая термодинамика является строгой теорией, развиваемой на основе нескольких постулатов. Однако обоснование этих постулатов и их связь со свойствами и законами взаимодействия частиц, из которых построены термодинамические системы, даётся статистической физикой. Статистическая физика позволяет выяснить также и границы применимости термодинамики.
Законы термодинамики носят общий характер и не зависят от конкретных деталей строения вещества на атомарном уровне. Поэтому термодинамика успешно применяется в широком круге вопросов науки и техники, таких как энергетика, двигатели, фазовые переходы, химические реакции, явления переноса и даже чёрные дыры.
Термодинамика имеет важное значение для самых разных областей физики и химии, химической технологии, аэрокосмической техники, машиностроения, клеточной биологии, биомедицинской инженерии, материаловедения и находит своё применение даже в таких областях, как экономика.

Основные понятия термодинамики: термодинамическая система, рабочее тело, идеальный газ
2. Термодинамические системы.
Термодинамическая система – это часть материального мира, отделенная от окружающей среды реальными или воображаемыми границами и являющаяся объектом исследования термодинамики. Окружающая среда значительно больше по объему, и поэтому изменения в ней незначительны по сравнению с изменением состояния системы. В отличие от механических систем, которые состоят из одного или нескольких тел, термодинамическая система содержит очень большое число частиц, что порождает совершенно новые свойства и требует иных подходов к описанию состояния и поведения таких систем. Термодинамическая система представляет собой макроскопический объект.
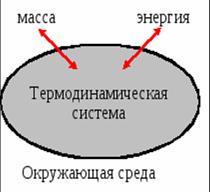
По типам связей с окружающей средой (по возможностям обмена с окружающей средой) ТДС бывает:.
Изолированная система не обменивается с окружающей ни энергией, ни веществом. Это идеализированная система, которую, в принципе нельзя экспериментально изучать.
Закрытая система может обмениваться с окружающей средой энергией, но не обменивается веществом.
Открытая система обменивается и энергией, и веществом
3. Состояние ТДС
3.1 Состояние ТДС – это совокупность всех ее измеримых макроскопических свойств, имеющих, следовательно, количественное выражение. Макроскопический характер свойств означает, что их можно приписать только к системе в целом, а не отдельным частицам, которые составляют ТДС (Т, р, V, c, U, nk). Количественные характеристики состояния связаны между собой. Поэтому существует минимальный набор характеристик системы, называемых параметрами, задание которых позволяет полностью описать свойства системы. Количество этих параметров зависит от типа системы. В простейшем случае для закрытой гомогенной газовой системы в состоянии равновесия достаточно задать только 2 параметра. Для открытой системы кроме этих 2 характеристик системы требуется задать число молей каждого компонента.
Термодинамические переменные подразделяются:
- внешние, которые определяются свойствами и координатами системы в окружающей среде и зависят от контактов системы с окружением, например, масса и количество компонентов, напряженность электрического поля, число таких переменных ограничено;
- внутренние, которые характеризуют свойства системы, например, плотность, внутренняя энергия, число таких параметров неограниченно;
- экстенсивные, которые прямо пропорциональны массе системы или числу частиц, например, объем, энергия, энтропия, теплоемкость;
-интенсивные, которые не зависят от массы системы, например, температура, давление.
Параметры ТДС связаны между собой соотношением, которое носит название уравнение состояние системы.
Общий вид его f (p,V, T) = 0.
Одна из важнейших задач – найти уравнение состояния любой системы. Пока точное уравнение состояния известно лишь для идеальных газов (уравнение Клапейрона - Менделеева).
(1)
где R – универсальная газовая постоянная = 8.314 Дж/(моль.К) .
[p] = Па, 1атм = 1,013*105 Па = 760 мм рт.ст.,
[V] = м3, [T] = К, [n] = моль, N = 6.02*1023 моль-1.
Реальные газы лишь приближенно описываются данным уравнением, и чем выше давление и ниже температура, тем больше отклонение от данного уравнения состояния.
3.2 Равновесное и неравновесное состояние ТДС
Различают равновесное и неравновесное состояния ТДС.
Классическая термодинамика обычно ограничивается рассмотрением равновесных состояний ТДС.
Равновесие - это такое состояние, к которому самопроизвольно приходит ТДС, и в котором она может существовать бесконечно долго в отсутствие внешних воздействий. Для определения равновесного состояния всегда требуется меньшее количество параметров, чем для неравновесных систем.
Равновесное состояние подразделяют на:
- устойчивое (стабильное) состояние, при котором всякое бесконечно малое воздействие вызывает только бесконечно малое изменение состояния, а при устранении этого воздействия система возвращается в исходное состояние;
- метастабильное состояние, при котором некоторые конечные воздействия вызывают конечные изменения состояния, которые не исчезают при устранения этих воздействий.
3.3 Термодинамический процесс
Изменение состояния ТДС связанное с изменением хотя бы одной из ее термодинамических переменных, называют термодинамическим процессом. Особенностью описания термодинамических процессов является то, что они характеризуются не скоростями изменения свойств, а величинами изменений. Процесс в термодинамике – это последовательность состояний системы, ведущая от начального набора термодинамических параметров к - конечному. Различают следующие термодинамические процессы:
- самопроизвольные, для осуществления которых не надо затрачивать энергию;
- несамопроизвольные, происходящие только при затрате энергии;
- необратимые (или неравновесные) – когда в результате процесса невозможно возвратить систему к первоначальному состоянию.
-обратимые – это идеализированные процессы, которые проходят в прямом и обратном направлении через одни и те же промежуточные состояния, и после завершения цикла ни в системе, ни в окружающей среде не наблюдается никаких изменений.
3.4 Функции состояния – это характеристики системы, которые зависят только от параметров состояния, но не зависят от способа его достижения.
Функции состояния характеризуются следующими свойствами:
- бесконечно малое изменение функции f является полным дифференциалом df;
- изменение функции при переходе из состояния 1 в состояние 2 определяется только этими состояниями ∫ df = f2 – f1
- в результате любого циклического процесса функция состояния не изменяется, т.е. равна нулю.
Теплота и работа – способы обмена энергией между ТДС и окружающей средой. Теплота и работа характеристики процесса, они не являются функциями состояния.
Работа - форма обмена энергией на макроскопическом уровне, когда происходят направленное перемещение объекта. Работа считается положительной, если ее совершает система против внешних сил.
Теплота – форма обмена энергией на микроскопическом уровне, т.е. в форме изменения хаотического движения молекул. Принято считать положительной теплоту, полученную системой, и работу, совершенную над ней, т.е. действует “эгоистический принцип”.
Наиболее часто используемыми единицами измерения энергии и работы, в частности, в термодинамике являются джоуль (Дж) в системе СИ и внесистемная единица – калория (1 кал = 4,18 Дж).
4. Параметры термодинамической системы
Совокупность макроскопических тел, которые при взаимодействии обмениваются энергией между собой и окружающей средой, называют термодинамической системой.
Взаимодействие в физике – воздействие тел или частиц друг на друга, приводящее к изменению состояния их движения.
Физические величины (например, давление, температура и т. д.), характеризующие состояние термодинамической системы в данный момент времени, называют параметрами состояния, или термодинамическими параметрами.
Число независимых параметров состояния равно числу степеней свободы термодинамической системы.
Различают параметры состояния физической системы экстенсивные, т. е. пропорциональные массе системы (объем, внутренняя энергия, свободная энергия, энтропия, термодинамические потенциалы и другим видам энергий), и интенсивные, независящие от массы (давление, температура и прочие).
Рассмотрим некоторые из них.
1) Количество вещества и постоянная Авогадро. Количество вещества наиболее естественно было бы измерять числом молекул или атомов в теле. Но число молекул в любом макроскопическом теле так велико, что в расчетах используют не абсолютное число молекул, а относительное их число.
В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль).
Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0,012 кг углерода 12C. Молекула углерода состоит из одного атома.
Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул).
Это число называется постоянной Авогадро NА:
NА = 6,02·1023 моль–1
Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА:
(2)
Массу одного моля вещества принято называть молярной массой μ.
2) Молярная масса равна произведению массы m0 одной молекулы данного вещества на постоянную Авогадро:
μ = NА · m0 (3)
Молярная масса выражается в килограммах на моль (кг/моль). Для веществ, молекулы которых состоят из одного атома, часто используется термин атомная масса.
Молярные массы всех химических элементов точно измерены и представлены в таблице Менделеева.
Складывая молярные массы элементов, входящих в состав молекулы вещества, можно вычислить молекулярную массу вещества. Например, молекулярная масса углекислого газа С02 приближенно равна 44, так как относительная атомная масса углерода точно равна 12, а кислорода примерно 16: 12 + 2 • 16 = 44.
Масса m любого количества вещества равна произведению массы одной молекулы на число молекул в теле: m = N · m0 (4) , где QUOTE m0 -масса молекулы.
3) Число молекул равно:
,
концентрация молекул n=N/V (6)
Учитывая формулу (2) и (5), количество вещества определяется:
(7)
Также количество вещества можно найти по формуле:
.
(8),
где Vm – молярный объем. Vm = 22,4*10-3 м3.
Плотность
вещества: (9)
Удельный объем - величина обратная плотности т.е. отношения объема занятого веществом к его массе.
4) Давление – физическая величина, характеризующая интенсивность сил, с которыми одно тело действует нормально (перпендикулярно) на поверхность другого – внутренний параметр системы.
При равномерном распределении силы по поверхности давление находится по формуле
.
В СИ единицей измерения давления считается паскаль (Па), 1 Н/м2 = 1 Па.
На практике традиционно используют некоторые внесистемные единицы.
Например, 1 бар = 105 10×Па, 1 ат = 9,81× 104 Па (техническая атмосфера),
1 мм рт. ст.= 1,33× 102Па, 1атм =1,033 ат =105 Па (нормальная атмосфера).
Для измерения давления используют манометры, барометры, вакуумметры, а также различные датчики давления.
Виды измеряемого давления:
1. Барометрическое (атмосферное) В - давление, измеряемое барометрами.
2. Манометрическое (превышающее атмосферное)
Рис. Схема манометра.
Давление газа в сосуде называется абсолютным (Рабс ).
Превышение давления в сосуде над барометрическим называется избыточным ( Ризб ).
Уравнение равновесия по сечению АС следующее Рабс = В + Ризб
3. Давление в вакууме (ниже атмосферного)
Схема вакуумметра.
Превышение барометрического давления над давлением в сосуде называется разрежением (Рр ).
Уравнение равновесия по сечению АС следующее Ра = В - Рр
Примеры решения задач
Задача 1. Найти абсолютное давление пара в котле, приведенное к 0ºС, если манометр показывает р = 0,13 МПа, а атмосферное давление по ртутному барометру составляет 680 мм рт. ст. (90660 Па) при температуре t = 25 ºС.
Дано:
Рман = 0,13·106 Па
В = Ратм = 90660 Па
Решение:
1) Из уравнения рабс = ратм + рман.
2) Показание барометра, полученное при t = 25 ºС приводим к 0 ºС.
В0 = В(1 – 0,000172t) = 90660·0,9957 = 90270 Па = 0,9 ·106 Па
3) Тогда абсолютное давление пара в котле
рабс = 0,13 + 0,09 = 0,22 МПа.
Задача 2. Избыточное давление в паровом котле Ризб1 = 0,04 МПа при барометрическом давлении Ратм1 = 96660 Па (725 мм рт. ст.). Чему будет равно избыточное давление в котле, если показание барометра повысится до Ратм2 = 104660 Па, а состояние пара в котле останется прежним? Барометрическое давление приведено к 0 ºС.
Дано:
Ризб1 = 0,4 бар
Ратм1 = 725 мм рт. ст.
Ратм2 = 785 мм рт. Ст
Ризб2 -?
Решение: Абсолютное давление в котле: ризб = рабс – рат.
рабс = ризб + рат.
рабс = 40000 + 96660 = 136660 Па.
Избыточное давление при показании барометра Ратм2 = 104660 Па.
Ризб = 136660 – 104660 = 32000 Па.
Задача 3. Давление воздуха по ртутному барометру равно 770 мм при 0°С. Выразить это давление в барах и паскалях.
Решение:
1мм рт.ст. = 133,3Па; 770мм рт.ст. =102700Па = 1,027бар.
Задача 4. В сосуде объемом 0,9м3 находится 1,5 кг окиси углерода (СО). Определить удельный объем и плотность окиси углерода.
Дано:
V = 0,9м3
m = 1,5 кг
v -?
ρ -?
Решение:
Задача 5. 0,5 м3 воздуха находится в сосуде при температуре 120 0С. Подключенный к сосуду вакуумметр показывает разрежение 700 мм вод. ст. при барометрическом давлении 750 мм рт. ст. Определить массу газа в сосуде.
Решение: Давление ниже атмосферного, поэтому
абсолютное давление газа pабм = B- pв = 750∙133,3-700∙9,81 = 93108 Па
Решение задач
1. Определить число атомов, содержащихся при нормальных условиях: 1) в 1г гелия; 2) 1г полностью диссоциированного азота; 3) в 1 м3 аргона.
2. Зная постоянную Авогадро, найти массу молекулы и атома водорода.
3. Сколько молекул содержится в углекислом газе (С02) массой 1 г?
4. В сосуде объемом 0,9м3 находится 1,5 кг окиси углерода (СО). Определить удельный объем и плотности окиси углерода.
5. Давление воздуха по ртутному барометру равно 670 мм при 0°С. Выразить это давление в барах и паскалях.
Задание 2.
Контрольные вопросы:
1. Что изучает термодинамика?
2. Какие области термодинамики вы изучали на занятиях общей физики?
3. Что такое термодинамическая система?
4. Что вы понимаете под термодинамическим процессов
5. Какие параметры термодинамической системы вам известны.
Домашнее задание:
Решите задачи:
1. Внесистемные единицы измерения давления 1 мм вод. ст. и 1мм рт. ст. выразить в н/м² ( на уровне моря ).
2. Давление по манометру в паровом котле составляет 9бар. Каково абсолютное давление в котле, если атмосферное давление по ртутному барометру равно 96500Па при температуре t = 20 ºС?
,