Строение атомного ядра. Ядерные силы
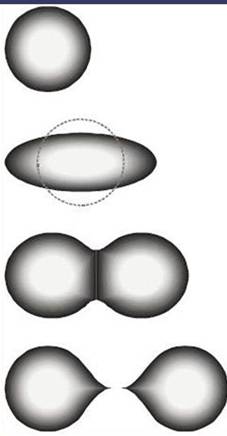
Капельная модель ядра
Первой моделью ядра была капельная модель, развитая в работах Н. Бора, Дж. Уиллера и Я. Френкеля. В этой модели атомное ядро рассматривается как сферическая капля заряженной жидкости.

Рисунок – Механизм деления ядра на основе капельной модели
Протонно-нейтронная модель ядра.
Сразу же после того, как в опытах Чедвика был открыт нейтрон, советский физик Д. Д. Иваненко и немецкий ученый В. Гейзенберг в 1932 г. предложили протонно-нейтронную модель ядра. Она была подтверждена последующими исследованиями ядерных превращений и в настоящее время является общепризнанной.
Согласно протонно-нейтронной модели ядра состоят из элементарных частиц двух видов — протонов и нейтронов.
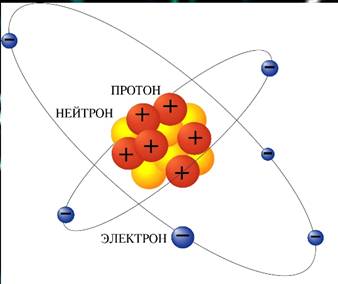

Состав атомного ядра
Так как в целом атом электрически нейтрален, а заряд протона равен модулю заряда электрона, то число протонов в ядре равно числу электронов в атомной оболочке. Следовательно, число протонов в ядре равно атомному номеру элемента Z в периодической системе элементов Д. И. Менделеева.
Заряд ядра равен Ze, где e – элементарный заряд. Число нейтронов обозначают символом N.
Общее число нуклонов (т. е. протонов и нейтронов) называют массовым числом A: A = Z + N
Ядра химических элементов обозначают символом A ZX , где X – химический символ элемента. Например,
1 1H – водород, – 4 2He - гелий,
Тогда число нейтронов в ядре N может быть найдено по разности между массовым числом и атомным номером:
N = A – Z
Изотопы и изобары
Массы протона и нейтрона близки друг к другу, и каждая из них примерно равна атомной единице массы. Масса электронов в атоме много меньше массы его ядра. Поэтому массовое число ядра равно округленной до целого числа относительной атомной массе элемента. Массовые числа могут быть определены путем приближенного измерения массы ядер приборами, не обладающими высокой точностью.
Ядра одного и того же химического элемента могут отличаться числом нейтронов. Такие ядра называются изотопами. У большинства химических элементов имеется несколько изотопов.
Например, у водорода их три:
1 1H обычный водород ,
2 1H – дейтерий
3 1H – тритий
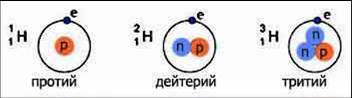
Изотопы представляют собой ядра с одним и тем же значением зарядового числа, но с различными массовыми числами А, т. е. с различными числами нейтронов N.
Химические элементы в природных условиях обычно представляют собой смесь изотопов. Существование изотопов определяет значение атомной массы природного элемента в периодической системе Менделеева. Так, например, относительная атомная масса природного углерода равна 12,011
Среди изотопов различных элементов были найдены такие, которые содержат в ядре при разном числе протонов одинаковое общее число нуклонов, то есть атомы которых обладают одинаковой массой. Такие изотопы были названы изобарами (от греческого слова “барос”, что означает “вес”). Различная химическая природа изобаров убедительно подтверждает то, что природа элемента обуславливается не массой его атома.
Ядерные силы. Так как ядра весьма устойчивы, то протоны и нейтроны должны удерживаться внутри ядра какими-то силами, причем очень большими. Что это за силы? Сразу можно сказать, что это не гравитационные силы, которые слишком слабые. Устойчивость ядра не может быть объяснена также электромагнитными силами, так как между одноименно заряженными протонами действует электрическое отталкивание. А нейтроны не имеют электрического заряда.
Значит, между ядерными частицами — протонами и нейтронами (их называют нуклонами) — действуют особые силы, называемые ядерными силами.
Свойства ядерных сил
1. Ядерные силы примерно в 100 раз превышают электрические (кулоновские) силы. Это самые мощные силы из всех существующих в природе. Поэтому взаимодействия ядерных частиц часто называют сильными взаимодействиями.
Сильные взаимодействия проявляются не только во взаимодействиях нуклонов в ядре. Это особый тип взаимодействий, присущий большинству элементарных частиц наряду с электромагнитными взаимодействиями.
2. Другая важная особенность ядерных сил — их короткодействие. Электромагнитные силы сравнительно медленно ослабевают с увеличением расстояния. Ядерные силы заметно проявляются лишь на расстояниях, равных размерам ядра (10-12—10-13 см), что показали уже опыты Резерфорда по рассеянию - частиц атомными ядрами. Ядерные силы — это, так сказать, «богатырь с очень короткими руками». Законченная количественная теория ядерных сил пока еще не разработана. Значительные успехи в ее разработке были достигнуты совсем недавно — в последние 10—15 лет.
Ядра атомов состоят из протонов и нейтронов. Эти частицы удерживаются в ядре ядерными силами.
Вывод:
ЯДЕРНЫЕ СИЛЫ
- это силы притяжения;
- действуют между всеми нуклонами в ядре;
- короткодействующие.
Энергия связи
Под энергией связи атомного ядра понимают энергию, которую нужно затратить, чтобы расщепить ядро на отдельные нуклоны. Такая же энергия выделяется при образовании ядра из свободных нуклонов.
Ее можно рассчитать, пользуясь формулой А. Эйнштейна, связывающей массу частицы и энергию:
Е=mc2
После создания масс-спектрографа можно было с большой точностью (до 0,01 %) измерить массы всех изотопов элементов таблицы Менделеева, что и сделано учеными.
Анализ этих данных показывает, что для всех элементов масса покоя ядра меньше, чем сумма масс покоя составляющих его нуклонов, если последние находятся в свободном состоянии. Это различие может быть охарактеризовано величиной
Δm = Zmp + (A – Z)mN – mя , которая носит название дефекта масс.
Уменьшение массы при образовании ядра из свободных частиц означает, что при этом уменьшается энергия этой системы частиц на величину энергии связи
Есв = (Zmp + (A – Z)mN – mя)с2 ,
Энергия связи определяется величиной работы, которую нужно совершить для расщепления ядра на составляющие его нуклоны.
Но куда расходуется эта энергия?
При образовании ядра из нуклонов последние за счет действия ядерных сил на малых расстояниях устремляются друг к другу с огромными ускорениями. Излучаемые при этом γ-кванты обладают энергией связи Есв, т.е. при образовании ядер из нуклонов эта энергия связи выделяется. Энергия связи очень велика (ее обычно выражают в МэВ: 1 МэВ = 106 эВ = = 1,6 ⋅10-13 Дж). Об этой величине можно судить по такому примеру: образование 4 г гелия сопровождается выделением такой же энергии, как при сгорании 5—6 вагонов каменного угля.
Удельная энергия связи
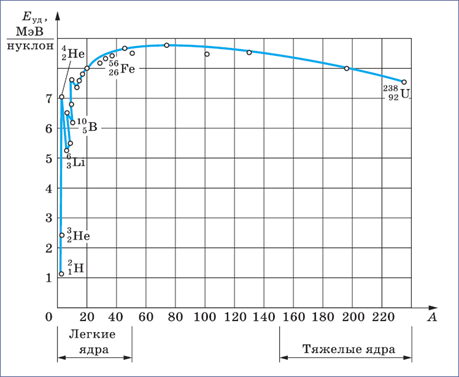
Важной характеристикой ядра служит средняя энергия связи ядра, приходящаяся на один нуклон (так называемая удельная энергия связи ядра), чем она больше, тем сильнее связаны между собой нуклоны, тем прочнее ядро. Эту удельную энергию связи εсв всегда можно подсчитать. Результаты показывают, что для большинства ядер εсв≈8 МэВ и уменьшается для очень легких и очень тяжелых ядер.
По мере увеличения числа нуклонов в ядре возрастают кулоновские силы отталкивания между протонами, ослабляющие связи в ядре, и величина εсв ядра у тяжелых ядер уменьшается. Величина εсв ядра максимальна у ядер средней массы (А = 50...60), следовательно, они отличаются наибольшей прочностью.
Примеры решения задач:
Задача 1. Каков состав ядер натрия 23 11Na, фтора 19 9F,
Решение:
1) Порядковый номер элемента показывает число протонов в ядре.
A ZX
23 11Na: Z= 11, следовательно 11 протонов
Число нейтронов находят вычитанием из массового числа порядкового номера.
N = A – Z = 23-11 =12 нейтронов;
2) 19 9F: Z= 9, следовательно 9 протонов
Число нейтронов находят вычитанием из массового числа порядкового номера.
N = A – Z = 19 - 9 = 10 нейтронов
Задача 2. Найти энергию связи ядра Есв и удельную энергию связи Есв/А для 2 1Н;
Масса ядра равна разности масс составляющих его нуклонов (протонов Z и нейтронов A – Z) и атомной массы элемента
m = Zmp + (A – Z)mN – mя
Энергия связи ядра равна энергии, которую требуется сообщить ядру для того, чтобы расщеплять его на нуклоны:
Есв = (Zmp + (A – Z)mN – mя)с2
Для изотопов H21
Есв = (1·1,00783 + (2 - 1)·1,00866 – 2,0141)·931,5=2,226 МэВ
Задачи для самостоятельного решения
1. Каков состав ядер натрия серебра 107 47Ag, кюрия 247 94Сm,
2. Каков состав изотопов неона 20 10Ne, 21 10Ne, 22 10Ne
3. Найти энергию связи ядра Есв и удельную энергию связи Есв/А для: 1) 6 3Li; 2) 7 3Li; 3) 12 6С.
4. Сколько нуклонов, протонов и нейтронов содержится в ядрах следующих элементов: 21 11Na, 9 4B, 16 8О, 14 7N, 127 13Al
Домашнее задание
Задачи:
1. Сколько нуклонов, протонов и нейтронов содержится в ядрах следующих элементов: 235U92 207Pb82
2. Чем отличаются следующие элементы: 17О8 и 16О8 235U92 и 239U92
Контрольные вопросы:
1. Какая модель ядра считается общепринятой в настоящий момент?
2. Каков состав ядра?
3. Что называется зарядовым и массовым числом?
4. Что называют ядерными силами?
5. Перечислите свойства ядерных сил?
6. Что называют энергией связи ядра?
7. Запишите формулу дефекта масс.