Законы термодинамики
Первый закон термодинамики
Первый закон термодинамики — это закон сохранения энергии, распространенный на тепловые явления. Он показывает, от каких причин зависит изменение внутренней энергии.
Падает, например, молот на кусок свинца, и свинец нагревается вполне определенным образом. Силы трения тормозят тела, которые при этом разогреваются.
На основании множества подобных наблюдений и обобщения опытных фактов был сформулирован закон сохранения энергии.
Энергия в природе не возникает из ничего и не исчезает: количество энергии неизменно, она только переходит из одной формы в другую.
Закон сохранения энергии управляет всеми явлениями природы и связывает их воедино. Он всегда выполняется абсолютно точно, неизвестно ни одного случая, когда бы этот великий закон не выполнялся.
В общем случае при переходе системы из одного состояния в другое внутренняя энергия изменяется одновременно как за счет совершения работы, так и за счет передачи теплоты. Первый закон термодинамики формулируется именно для таких общих случаев:
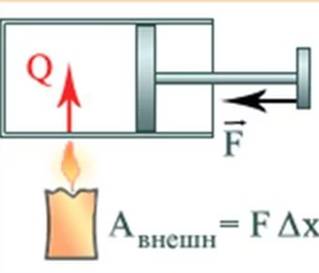
Изменение внутренней энергии системы при переходе ее из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе:
ΔU= A + Q (1)

Если система является изолированной, то работа внешних сил равна нулю (А = 0) и система не обменивается теплотой с окружающими телами (Q = 0). В этом случае согласно первому закону термодинамики ΔU = U2 – U1 = 0, или U1 = U2.
Внутренняя энергия изолированной системы остается неизменной (сохраняется).
Вместо работы А внешних тел над системой рассматривают работу А' системы над внешними телами.
Учитывая, что А' = - А, первый закон термодинамики (1) можно записать так:
Q = ΔU + A'. (2)
Количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами.
Невозможность создания вечного двигателя.
Из первого закона термодинамики вытекает невозможность создания вечного двигателя — устройства, способного совершать неограниченное количество работы без затрат топлива или каких-либо других материалов. Если к системе не поступает тепло (Q = 0), то работа А' согласно уравнению (2) может быть совершена только за счет убыли внутренней энергии: А' = —ΔU. После того как запас энергии окажется исчерпанным, двигатель перестанет работать.
Второй закон термодинамики
Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Его открыл в результате длительных исследований, завершившихся изданием собрания трудов в 1874 году, великий немецкий естествоиспытатель и врач Юлиус Роберт фон Майер.

Первый закон термодинамики позволяет определить количественные соотношения между различными формами энергии, которые принимают участие в данном процессе. Первый закон термодинамики показывает, что различные виды энергии могут превращаться друг в друга в эквивалентных количествах. Однако он ничего не говорит о том, в каком направлении будет происходить превращение энергии в системе, т. е. в каком направлении будет развиваться тот или иной процесс. Ответы на эти вопросы дает второй закон термодинамики, обоснованный Карно (1824), развитый Клаузисом (1850), Томсоном (1851), Больцманом (1880) и другими учеными.

Второй закон термодинамики: Невозможен переход теплоты от тела более холодного к телу более нагретому без каких-либо изменений в окружающей средой.
Пример решения задач:
Задача 1. Вычислить количество теплоты, переданное водороду массой 2кг при изохорном повышении температуры на 10 К.
Дано: Решение:
Задача 2. Водород массой m =0,66 кг изобарно нагрели на ΔТ=328К. Найти 1) работу А, совершенную газам; 2) количество теплоты Q, сообщенное газу; 3) изменение внутренней энергии
Задачи для самостоятельного решения:
1. Газ массой m изобарно нагрели на ΔТ. Найти 1) работу А, совершенную газам; 2) количество теплоты Q, сообщенное газу; 3) изменение внутренней энергии
|
Газ |
т, кг |
Д Т, к |
|
Азот |
0,51 |
81 |
|
Водород |
0,066 |
238 |
|
Воздух |
0,31 |
27 |
|
Гелий |
1,1 |
23 |
|
Кислород |
0,007 |
810 |
2. Для изобарного нагревания газа, количество вещества которого 800 моль, на 500 К ему сообщили количество теплоты 9,4 МДж. Определить работу газа и приращение его внутренней энергии.
3. Удельная теплоемкость азота, когда его нагревают при постоянном давлении, равна 1,05 кДж/(кг • К), а при постоянном объеме — 0,75 кДж/(кг • К). Почему эти величины имеют разные значения? Какая совершается работа при изобарном нагревании азота массой 1 кг на 1 К?
4. Идеальный газ получил количество теплоты, равное 300 Дж, и совершил работу, равную 100 Дж. Как изменилась внутренняя энергия газа?
А. увеличилась на 400 Дж
Б. увеличилась на 200 Дж
В. уменьшилась на 400 Дж
Г. уменьшилась на 200 Дж
5. Идеальный газ совершил работу, равную 100 Дж, и отдал количество теплоты, равное 300 Дж. Как при этом изменилась внутренняя энергия?
А. увеличилась на 400 Дж
Б. увеличилась на 200 Дж
В. уменьшилась на 400 Дж
Г. уменьшилась на 200 Дж
6. Идеальный газ совершил работу, равную 300 Дж. При этом внутренняя энергия уменьшилась на 300 Дж. Каково значение количества в этом процессе?
А. отдал 600 Дж
Б. отдал 300 Дж
В. получил 300 Дж
Г. не отдавал и не получал теплоты.
7. Идеальный газ совершил работу, равную 300 Дж. При этом его внутренняя энергия увеличилась на 300 Дж. Какое количество теплоты получил газ?
А. отдал 600 Дж
Б. отдал 300 Дж
В. получил 600 Дж
Г. получил 300 Дж
Составить план изучения закона
Пункты плана:
1. Связь между какими величинами выражает данный закон?
2. Формулировка закона и математическая запись закона.
3. Когда и кто впервые сформулировал данный закон?
4. Опыты, подтверждающие справедливость закона.
5. Учёт и использование закона на практике.
6. Границы применимости закона
Домашнее задание:
Задачи:
1. Объем кислорода массой 160 г, температура которого 27 °С, при изобарном нагревании увеличился вдвое. Найти работу газа при расширении, количество теплоты, которое пошло на нагревание кислорода, изменение внутренней энергии.
2. Во сколько раз количество теплоты, которое идет на нагревание газа при постоянном давлении, больше работы, совершаемой газом при расширении? Удельная теплоемкость газа при постоянном давлении ср, молярная масса М.
Контрольные вопросы:
1. Как формулируется первый закон термодинамики?
2. В каком случае изменение внутренней энергии отрицательно?
3. Почему можно говорить, что система обладает внутренней энергией, но нельзя сказать, что она обладает запасом определенного количества теплоты или работы?