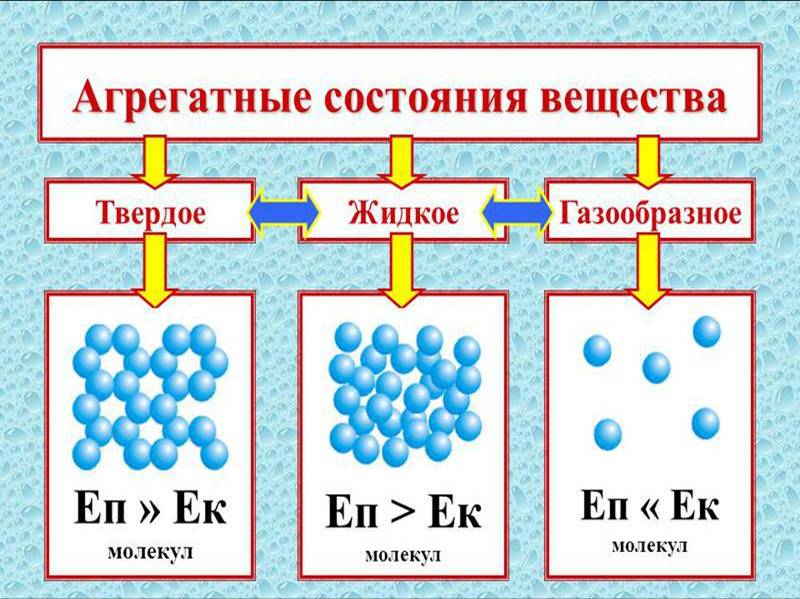
Изменение агрегатных состояний вещества.
Агрегатные состояния
Всякое вещество может находиться в трёх агрегатных состояниях: в твёрдом, жидком и газообразном.
В газах средняя кинетическая энергия теплового движения молекул значительно превосходит потенциальную энергию их взаимодействия. В этом случае силы взаимодействия между молекулами весьма слабо влияют на характер их относительного движения, поскольку молекулы находятся на достаточно большом расстоянии друг от друга. По мере уменьшения температуры или при сжатии взаимодействие молекул начинает играть настолько существенную роль, что газ в конце концов переходит в конденсированное состояние - жидкость.
В жидкости средняя энергия взаимодействия молекул примерно равна средней энергии теплового движения. Тепловое движение нарушает связь между молекулами и приводит к перемещению их относительно друг друга внутри объёма жидкости. В связи с этим жидкость принимает форму сосуда, в который она помещена.
Под твердыми телами обычно подразумеваются кристаллы, характерной особенностью которых является регулярное расположение в них атомов или ионов. О совокупности точек, в которых расположены атомные ядра, говорят как о кристаллической решетке, а сами эти точки называют узлами решетки.
Тепловое движение атомов или ионов кристалла носит в основном колебательный характер. Однако, поскольку в кристалле кинетическая энергия колебательного движения атомов значительно меньше абсолютного значения потенциальной энергии их взаимодействия, то тепловое движение не может разрушить связь между атомами. Поэтому твердое тело, в отличие от жидкости, сохраняет свою форму и обладает большой механической прочностью.
Кроме кристаллических тел существуют аморфные тела. Они, хотя и рассматриваются обычно как твердые, представляют собой переохлажденные жидкости. Если рассматривать некоторый атом аморфного тела как центральный, то ближайшие к нему атомы будут располагаться в определенном порядке, но по мере удаления от "центрального" атома этот порядок нарушается и расположение атомов становится случайным. К аморфным телам относятся стекло, пластмассы и т.д.

Характер движения молекул в твердых, жидких и газообразных тел.
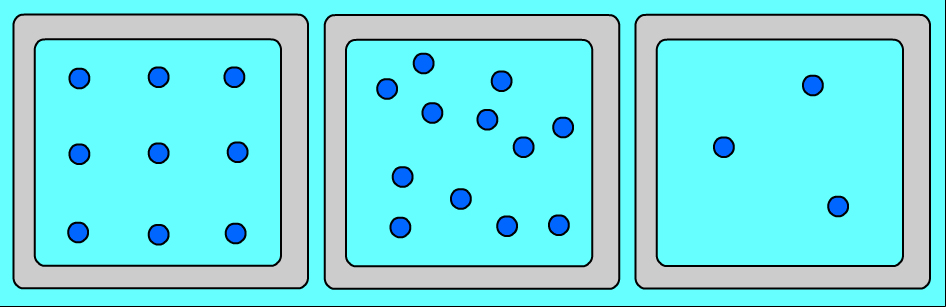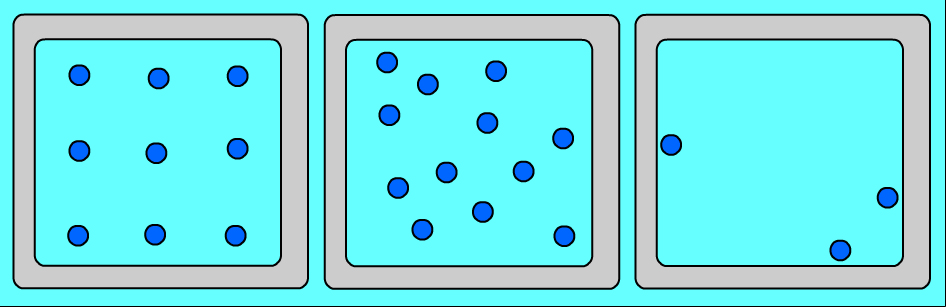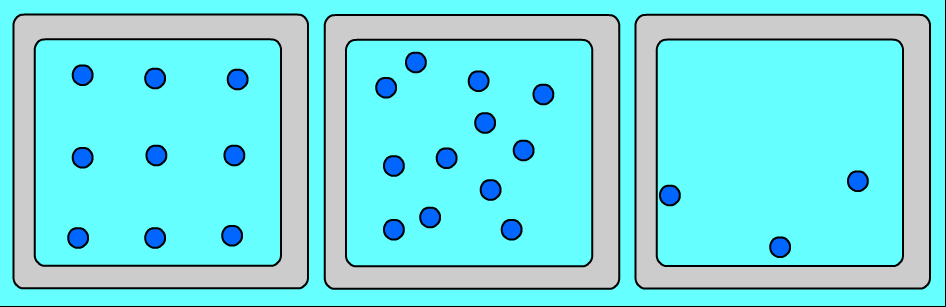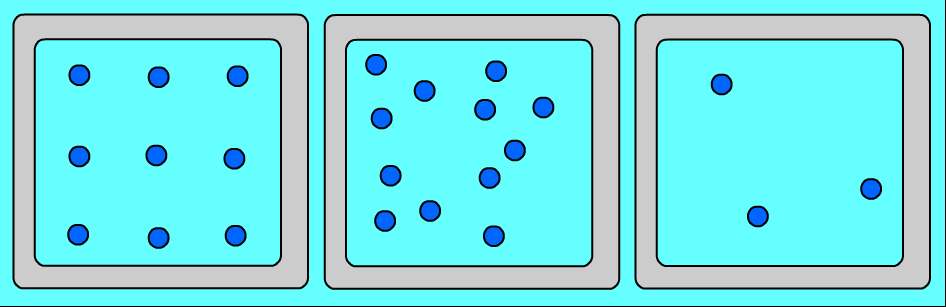
Переход из одного агрегатного состояния в другое (при постоянном давлении) происходит при строго определённой температуре и всегда связан с выделением или поглощением некоторого количества тепла. Переход вещества из одного состояния в другое происходит не мгновенно, а в течении некоторого времени, когда два состояния вещества существуют одновременно в тепловом равновесии.
Плавление и кристаллизация
По мере возрастания температуры энергия колебательного движения атомов в твёрдом теле возрастает и, наконец, наступает такой момент, когда связи между атомами начинают разрываться. При этом твердое тело переходит в жидкое состояние. Такой переход называется плавлением. При фиксированном давлении плавление происходит при строго определённой температуре.
Количество тепла, необходимое для превращения единицы массы вещества в жидкость при температуре плавления, называют удельной теплотой плавления λ.
Для плавления вещества массой m необходимо затратить количество теплоты равное:
Q = λ·m. (1)
Плавление льда. Температура в процессе плавления не меняется
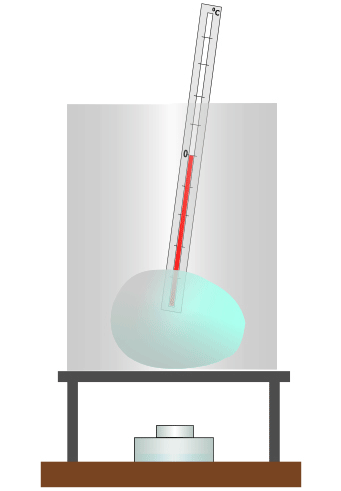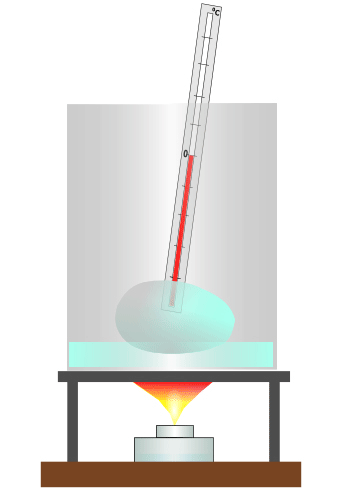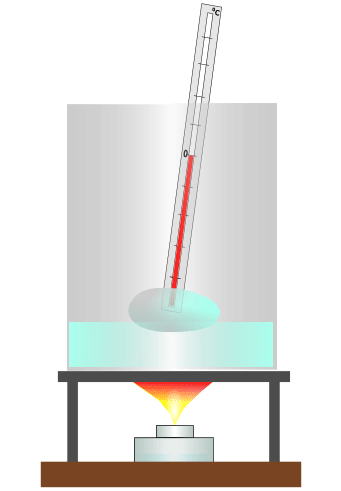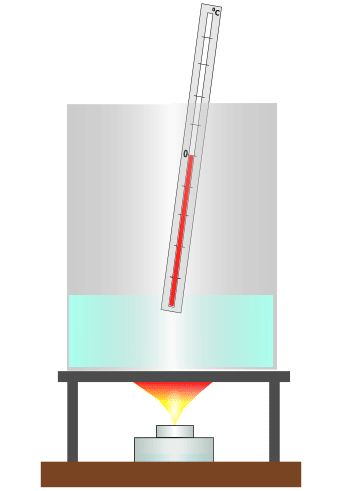
При охлаждении расплавленного твёрдого тела происходит обратный процесс, называемый кристаллизацией. Образование кристалла также происходит при постоянной температуре, равной температуре плавления. При кристаллизации жидкости выделяется такое же количество теплоты, какое поглощается при плавлении вещества той же массы.
Q = - λ·m. (2)
Кристаллизация перенасыщенного раствора ацетата натрия

Аморфные тела в противоположность кристаллам не имеют определенной температуры плавления.
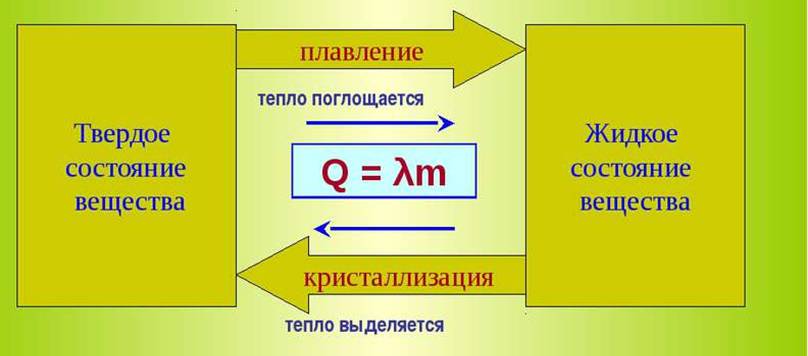
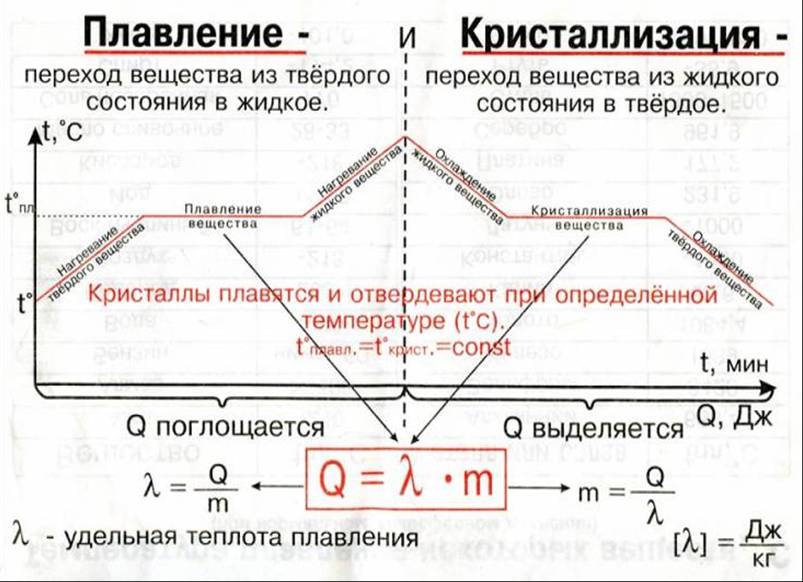
График плавления и кристаллизации
Испарение и конденсация.
Как в жидкостях, так и в твердых телах всегда имеется некоторое число молекул, энергия которых достаточна для преодоления притяжения к другим молекулам и которые способны оторваться от поверхности жидкости или твердого тела и перейти в окружающее их пространство. Этот процесс для жидкости называется испарением (или парообразованием), а для твердых тел - сублимацией (или возгонкой).
Испарение – это процесс перехода вещества из жидкого в газообразное.
Количество тепла Q, которое необходимо сообщить жидкости для испарения единицы её массы при постоянной температуре, называется удельной теплотой парообразования r.
Количество теплоты, которое надо затратить, чтобы перевести в пар жидкость массой m,
Q = r·m. (3)
В результате хаотического движения над поверхностью жидкости молекула пара, попадая в сферу действия молекулярных сил, вновь возвращается в жидкость. Этот процесс называется конденсацией.
Конденсация – это процесс перехода вещества в жидкое их газообразного
Q = - r·m. (4)
Испарение жидкости происходит при любой температуре и тем быстрее, чем выше температура, больше площадь свободной поверхности испаряющейся жидкости и быстрее удаляются образовавшиеся над жидкостью пары.
Следует обратить внимание, что процесс парообразования связан с увеличением внутренней энергии вещества, а процесс конденсации - с уменьшением ее.
Схема испарения и конденсации
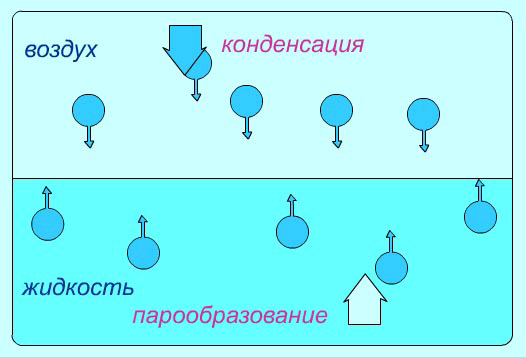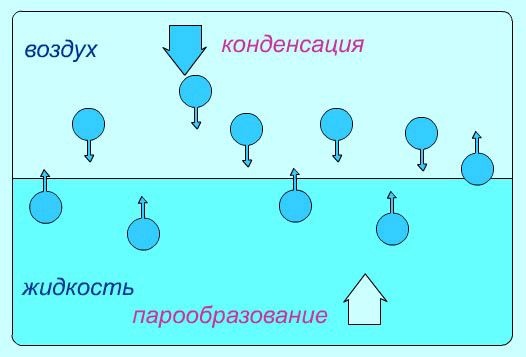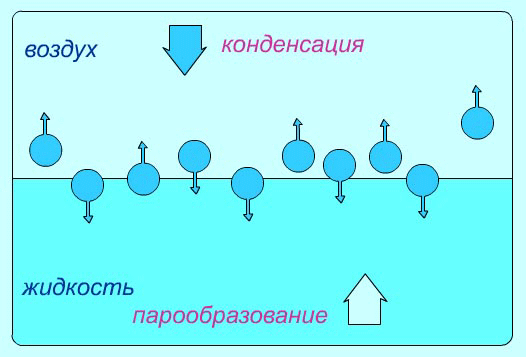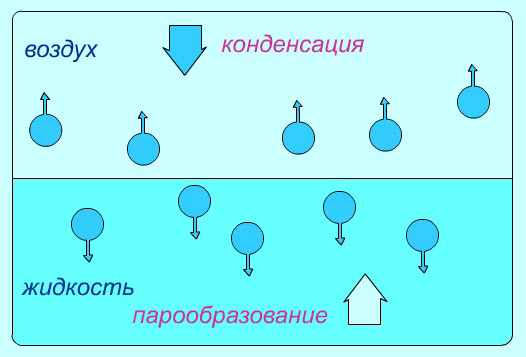
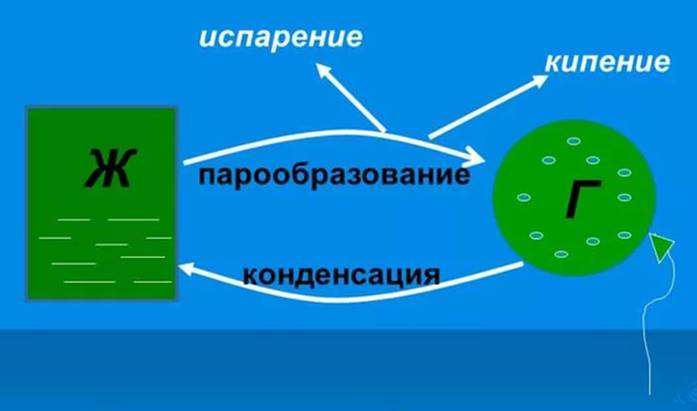
График парообразования и конденсации
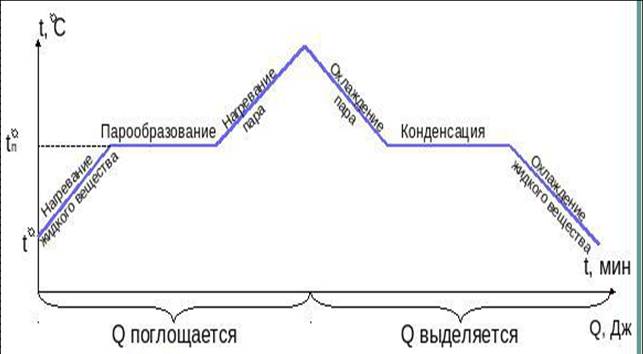
Нагревание и охлаждение.
Для нагревания тела массой массой m от температуры t1 до температуры t2 необходимо передать ему количество теплоты
Q = cm (t2- t1) (5)
При остывании теле его конечная температура оказывается меньше начальной и количество теплоты, отдаваемое телом, отрицательное
Q = - cm (t2- t1) (6)
Коэффициент с в формуле называется удельной теплоемкостью вещества.
Удельная теплоемкость – это величина численно равная количеству теплоты, которое получает или отдает вещество массой 1 кг при изменении его температура на 1 К.
Контрольное задание:
Задание 1:
Закончите фразу:
1. Процесс перехода вещества из твёрдого состояния в жидкое называется ……….
2. Обратный процесс плавлению это - …………
3. Физическая величина, показывающая какое количество теплоты необходимо затратить, чтобы 1 кг твёрдого вещества, находящего при температуре плавления превратить в жидкость, называется ……………, обозначается буквой ………., её единица измерения ……….
4. Напишите формулу для расчёта количества теплоты, которая выделяется при кристаллизации вещества произвольной массы …………
5. Процесс перехода вещества из газообразного состояния в жидкое называется ……..
6. Напишите два вида парообразования …………………….
7. Напишите формулу для расчёта количества теплоты, необходимого для превращения в пар жидкости произвольной массы, взятой при температуре плавления ………
Задание 2:
1.
Проанализируйте график и ответьте на следующие вопросы: в какие промежутки
времени температура вещества изменялась и как? В какие промежутки времени она
оставалась постоянной и почему? Какой из участков графика соответствует
отвердеванию вещества? Охлаждению после кристаллизации?
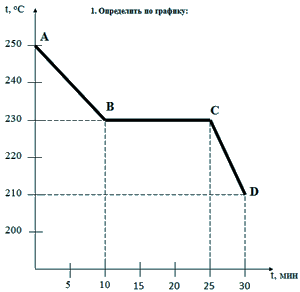
2. Найдите по графику в каком состоянии находилось вещество через 3 мин после начала охлаждения? Через 5 мин? Через 8 мин? Через 10 мин? Какая точка графика соответствует началу кристаллизации вещества? В течение какого промежутка времени вещество отвердевало? Какой была при этом его температура?

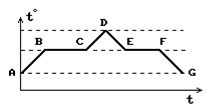
3. Используя изображенный на рисунке график изменения температуры олова, определите, какие участки этого графика соответствуют плавлению олова, нагреванию олова до точки плавления, отвердеванию, охлаждению жидкого олова до точки плавления, нагреванию жидкого олова, охлаждению твердого олова
Примеры решения задач
Задача 1. Сколько теплоты выделится при конденсации 200 г водяного пара, имеющего температуру 1000С, и при охлаждении полученной воды до 200С.
Дано: Решение:
m = 0,2 кг Общее количество теплоты будет складываться из
t1 = 1000C количества теплоты двух процессов: конденсации пара и охлаждения
t2 = 200C воды.
Q-? Q = Q2 + Q1
При конденсации пара Q1 = - r·m = - 2,26·106 ·0,2 = - 0,452·106Дж.
При охлаждении пара Q2 = - cm (t1- t2) = - 4,2·103·0,2(100-20) = - 67,2·103 = - 0,067·106Дж
Q = Q2 + Q1 = - 0,452·106 - 0,067·106 = - 0,519 ·106 Дж
Ответ: - 0,519 ·106 Дж
Задача 2.
Задачи для самостоятельного решения:
1. Два шарика равной массы медный и алюминиевый, сброшены с высоты 1000 м Который из них нагреется больше и насколько? Потери тепла не учитывать.
2. На сколько градусов нагреется при штамповке кусок стали массой 1,5 кг от удара молота массо1 392 кг, если скорость молота в момент удара 7 м/с, а на нагревание стали затрачивается 60% энергии молота?
3. Стальной молот массой 12 кг падает на лежащую на наковальне железную пластину массой 0,2 кг. Высота падения молота 1,5 кг. Считая, что на нагревание пластины затрачивается 40% кинетической энергии молота, вычислить, на сколько градусов нагреется пластина после 50 ударов молота.
4. Сколько теплоты выделится при конденсации 300 г водяного пара, имеющего температуру 1000С, и при охлаждении полученной воды до 600С.
5. Сколько тепла нужно затратить, чтобы расплавить: 1) 100 г льда при температуре 00С? 2) 100 г льда при температуре – 200С?
6. Какое количество тепла нужно затратить, чтобы 6 кг льда при температуре – 200С обратить в пар с температурой 1000С?
Домашнее задание:
Контрольные вопросы:
1. От чего зависит удельная теплоемкость вещества?
2. Что называют удельной теплотой парообразования?
3. Что называют удельной теплотой плавления?
4. В каких случаях количество теплоты положительная величина, а в каких случаях
отрицательная?
Задачи:
1. Какое количество водяного пара, взятого при температуре 1000 С, потребуется для нагревания бетонной плиты массой 200 кг от температуры 100 С до температуры 400 С? (2,3 кг)
2. Определите, какая температура установится в сосуде после таяния льда, если в воду массой 200 г, взятую при температуре 600 С, добавить лед массой 20 г при температуре 00 С. (47,2 С)
3. Определите количество теплоты, которое выделяется при конденсации эфира массой 8 г, имеющего температуру 350 С. (3200Дж)