Лабораторная работа №6 «Изучение закона Бойля-Мариотта»
(Лабораторная работа - дистанционная выполняется в домашних условиях)
Цель работы: проверить на опыте закон Бойля-Мариотта.
Задание 1 (1 балл):
1. Ответить на вопросы
А. Запишите определение, формулу изотермического процесса, постройте изотерму
Б. Запишите определение, формулу изобарного процесса, постройте изобару.
В. Запишите определение, формулу изохорного процесса, постройте изохору.
Г. Запишите уравнение Менделеева-Клайперона
Д. Запишите основное уравнение МКТ.
Задание 2: Проверить выполнение закона экспериментально (3 балла):
Оборудование: прибор для изучения газовых законов, барометр, испытуемый газ — воздух.
Описание установки.
Прибор состоит из шприца (1), вмонтированного в стакан (2) и манометра (3).
Выход шприца соединяют длинными трубками (5) через тройник (6) с манометром.
Свободный конец тройника служит для соединения с атмосферой, на него надевают короткую трубку (8), которую при необходимости можно перекрыть зажимом (4).
Порядок выполнения работы:
1. При изменении объемы воздуха в баллоне, с помощью шприца, манометр фиксирует изменение давления. Результаты для объема и давления представлены в таблице (V, ΔP)
2. Показания манометра из мм.рт.ст необходимо перевести в Па и записать в таблицу.
1мм. рт. ст. = 133 Па
3. При расчете реального давления воздуха в баллоне, необходимо учитывать атмосферное давление Р0 = 10·104 Па.
Поэтому давление воздуха в баллоне найдем по формуле: Р1 = P0+ ΔP׀
Результаты занесите в таблицу
4. Рассчитайте постоянную для каждого опыта: с1 = P1 V1;
Например: с1 = 100·10-6 · 10·104 = 10 Па·м3
5.
Вычислите отношения
и
сравните, полученные результаты с единицей
6. Построить график зависимость давления от объема. По оси объем за две клеточки возьмите 10м3, по оси давления за две клеточки 10·104 Па.
7. Сделать вывод: выполняется ли закон Бойля-Мариотта
Подгруппа 1- Первые 13 человек по списку в журнале
Подгруппа 2 – Обучающиеся с порядковым номером 14 и ниже
Таблица. Подгруппа 1 Атмосферное давление P0 =10·104 , Па
|
№ |
Объем воздуха V, м3
|
Показания манометра ΔP, мм.рт.ст |
Показания манометра, ΔP, Па 1мм.рт.ст=133 Па |
Давление воздуха в шприце Р = P0+ΔP, Па |
Постоянная PV = с, Па м3 |
Отношения |
|
1 |
V1 = 100·10-6 |
0 |
ΔP= 0·133 = 0 |
Р1 = 10·104 + 0 = 10·104 |
P1V1 =10 |
|
|
2 |
V2 = 90·10-6 |
60 |
ΔP= 60·133 = |
Р2 = 10·104 + = |
P2V2 = |
|
|
3 |
V3 = 80·10-6 |
120 |
ΔP= 120·133= |
Р3 = 10·104 + = |
P3V3 = |
|
|
4 |
V4 = 70·10-6 |
184
|
ΔP= 184·133= |
Р4 = 10·104 + = |
P4V4 = |
|
|
5 |
V5 = 60·10-6 |
250 |
ΔP= 250·133= |
Р5 = 10·104 + = |
P5V5 = |
|
|
6 |
V6 = 50·10-6 |
320 |
ΔP= 320·133= |
Р6 = 10·104 + = |
P6V6 = |
|
Подгруппа 2
|
№ |
Объем воздуха V, м3
|
Показания манометраΔP, мм.рт.ст |
Показания манометра, ΔP, Па 1мм.рт.ст=133 Па |
Давление воздуха в шприце Р = P0+ΔP, Па |
Постоянная PV = с, Па м3 |
Отношения |
|
1 |
V1 = 80·10-6 |
0 |
ΔP= 0·133 = 0 |
Р1 = 10·104 + 0 = 10·104 |
P1V1 = 8 |
|
|
2 |
V2 = 70·10-6 |
65 |
ΔP= 65·133= |
Р2 = 10·104 + = |
P2V2 = |
|
|
3 |
V3 = 60·10-6 |
125 |
ΔP= 125·133= |
Р3 = 10·104 + = |
P3V3 = |
|
|
4 |
V4 = 50·10-6 |
190 |
ΔP= 190·133= |
Р4 = 10·104 + = |
P4V4 = |
|
|
5 |
V5 = 40·10-6 |
240 |
ΔP= 240·133= |
Р5 = 10·104 + = |
P5V5 = |
|
|
6 |
V6 = 30·10-6 |
280 |
ΔP= 280·133= |
Р6 = 10·104 + = |
P6V6 = |
|
Задание 3 (1 балл) При уменьшении абсолютной температуры в 3 раза, объем газа уменьшился на 20·10-6 м3. Найти первоначальный объем.
Критерии оценки
5 баллов – отлично 4 балла – хорошо
3 балла – удовлетворительно 1-2 балла – неудовлетворительно
Методические указания:
Пример1. В цилиндре дизельного двигателя автомобиля KAMA3-5320 температура воздуха в начале такта сжатия была 50 °С. Найти температуру воздуха в конце такта, если его объем уменьшается в 17 раз, а давление возрастает в 50 раз.
Пример 2. Какой объем займет газ при температуре 77°С, если при температуре 27°С его объем был 6 л?
Теория:
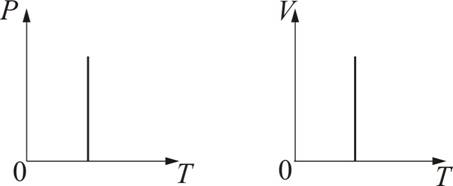
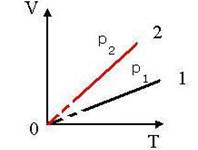
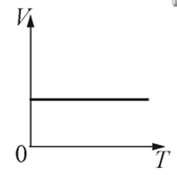
Графически изобарный процесс изображается прямой, которая называется изобарой.
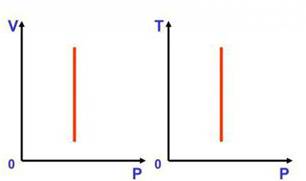
Изохорный процесс изображается прямой, называемой изохорой
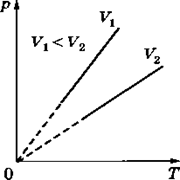
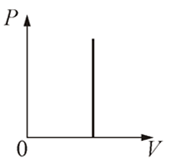
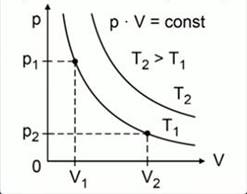
Зависимость давления газа от объема при постоянной температуре графически изображают кривой, которую называют изотермой.