Основные положения Молекулярно-кинетической теории (МКТ)
Основные положения МКТ
Молекулярно-кинетическая теория (сокращённо МКТ) — теория, возникшая в XIX веке и рассматривающая строение вещества, в основном газов, с точки зрения трёх основных приближенно верных положений:
- все тела состоят из частиц: атомов, молекул и ионов;
- астицы находятся в непрерывном хаотическом движении (тепловом);
- частицы взаимодействуют друг с другом путём абсолютно упругих столкновений.
МКТ стала одной из самых успешных физических теорий и была подтверждена целым рядом опытных фактов. Основными доказательствами положений МКТ стали:
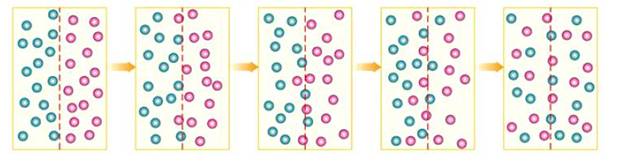
Диффузия. Тепловое движение. Броуновское движение.
Диффузия - перемешивание газов, жидкостей и твердых тел при их непосредственном контакте.


Броуновское движение — это тепловое движение взвешенных в жидкости (или газе) частиц.
Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение. Это тепловое движение мельчайших микроскопических частиц, взвешенных в жидкости или газе. Оно было открыто английским ботаником Р. Броуном в 1827 г. Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друг друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую.
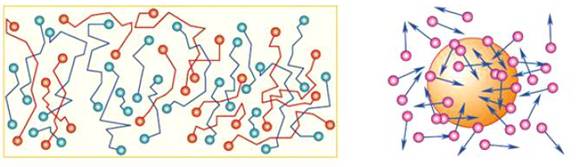

Теория броуновского движения была создана А. Эйнштейном в 1905 г. Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Ж. Перрена, проведенных в 1908–1911 гг.
Относительная молекулярная масса.
Так как массы молекул очень малы, удобно использовать в расчетах не абсолютные
значения масс, а относительные. По международному соглашению массы всех атомов
и молекул сравнивают с — массы атома углерода (так называемая углеродная шкала
атомных масс). Относительной молекулярной (или атомной) массой вещества
Мr
называют отношение массы молекулы (или атома)
т0 данного
вещества к 1/12 массы атома углерода.
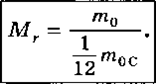 (1)
(1)
Количество вещества и постоянная Авогадро. Количество вещества наиболее естественно было бы измерять числом молекул или атомов в теле. Но число молекул в любом макроскопическом теле так велико, что в расчетах используют не абсолютное число молекул, а относительное их число.
В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль).
Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0,012 кг углерода 12C. Молекула углерода состоит из одного атома.
Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул).
Это число называется постоянной Авогадро NА: NА = 6,02·1023 моль–1
Постоянная Авогадро – одна из важнейших постоянных в молекулярно-кинетической теории.
Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА:
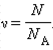
Массу одного моля вещества принято называть молярной массой M. Молярная масса равна произведению массы m0 одной молекулы данного вещества на постоянную Авогадро: μ = NА · m0 (3)
Молярная масса выражается в килограммах на моль (кг/моль). Для веществ, молекулы которых состоят из одного атома, часто используется термин атомная масса.
Молярные массы всех химических элементов точно измерены и представлены в таблице Менделеева.
Складывая молярные массы элементов, входящих в состав молекулы вещества, можно вычислить молекулярную массу вещества. Например, молекулярная масса углекислого газа С02 приближенно равна 44, так как относительная атомная масса углерода точно равна 12, а кислорода примерно 16: 12 + 2 • 16 = 44.
Масса m любого
количества вещества равна произведению массы одной молекулы на число молекул в
теле: ![]() (4) , где
m0 -масса
молекулы.
(4) , где
m0 -масса
молекулы.
Число молекул равно:
(5),
концентрация молекул
(6)
Учитывая формулу (2) и (5), количество вещества определяется:
(7)
Также количество вещества можно найти по формуле:
![]() (8),
(8),
где Vm – молярный объем.
Vm = 22,4·10-3 м3.
Плотность вещества:
(9)
Примеры решения задач:
Задача 1. Определить число молекул, находящиеся при нормальных условиях в: 1) 1г азота, 2) 1г углекислого газа, 3) в 1 м3 кислорода.
Задача 2. Найти массу атома водорода, гелия, хлора.
Задачи для самостоятельного решения:
1. Найти массу атомов гелия, хлора.
2. Зная, что диаметр молекулы кислорода равен 2,98·10-10 м, подсчитать какой длины получилась бы цепочка из молекул, находящихся в 0,5 см3 кислорода при нормальных условиях, если эти молекулы расположены вплотную в один ряд.
3. Определить число атомов, содержащихся при нормальных условиях: 1) в 1г гелия; 2) 1г полностью диссоциированного азота; 3) в 1 м3 аргона.
4. Зная постоянную Авогадро, найти массу молекулы и атома водорода.
5. Сколько молекул содержится в углекислом газе (С02) массой 1 г?
6. Найти число атомов в алюминиевом предмете массой 135 г.
7. На изделие, поверхность которого 20 см2, нанесен слой серебра толщиной 1 мкм. Сколько атомов серебра содержится в покрытии?
Домашнее задание:
Контрольные вопросы.
1.Чему равна относительная молекулярная масса воды?
2.Сколько молекул в двух молях воды?
Задачи
1. Какое количество вещества содержится в алюминиевой отливке массой 5,4 кг?
2. Какова масса 500 моль углекислого газа?
3. Какой объем занимают 100 моль ртути?
4. Сравнить массы и объемы двух тел, сделанных соответственно из олова и свинца, если в них содержатся равные количества вещества.